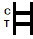การทดสอบอย่างรวดเร็วพรหม
การใช้งานที่ตั้งใจไว้
Strongstep®การทดสอบพรหมเป็นการทดสอบอิมมูโนโครมาโตกราฟีเชิงคุณภาพที่ตีความด้วยสายตาสำหรับการตรวจหา IGFBP-1 จากของเหลวน้ำคร่ำในการหลั่งช่องคลอดในระหว่างตั้งครรภ์ การทดสอบนี้มีไว้สำหรับการใช้งานอย่างมืออาชีพเพื่อช่วยวินิจฉัยการแตกของเยื่อหุ้มทารกในครรภ์ (ROM) ในหญิงตั้งครรภ์
การแนะนำ
ความเข้มข้นของ IGFBP-1 (ปัจจัยการเจริญเติบโตที่คล้ายอินซูลินจับโปรตีน -1) ในของเหลวน้ำคร่ำสูงกว่าในซีรั่มของมารดา 100 ถึง 1,000 เท่า IGFBP-1 มักจะไม่ปรากฏในช่องคลอด แต่หลังจากการแตกของเยื่อหุ้มเซลล์ของทารกในครรภ์ของเหลวน้ำคร่ำที่มีความเข้มข้นสูงของ IGFBP-1 ผสมกับการหลั่งช่องคลอด ในการทดสอบStrongstep® Prom ตัวอย่างของการหลั่งช่องคลอดจะถูกนำมาใช้กับ Swab โพลีเอสเตอร์ที่ผ่านการฆ่าเชื้อและตัวอย่างจะถูกสกัดลงในสารละลายการสกัดชิ้นงาน ตรวจพบการปรากฏตัวของ IGFBP-1 ในโซลูชันโดยใช้อุปกรณ์ทดสอบอย่างรวดเร็ว
หลักการ
Strongstep®การทดสอบพรหมใช้ Immunochromatographic, เทคโนโลยีการไหลของเส้นเลือดฝอย ขั้นตอนการทดสอบต้องการการละลายของ IGFBP-1 จากการล้างช่องคลอดโดยการผสม SWAB ในบัฟเฟอร์ตัวอย่าง จากนั้นบัฟเฟอร์ตัวอย่างผสมจะถูกเพิ่มเข้าไปในตัวอย่างเทปคาสเซ็ตและส่วนผสมจะอพยพไปตามพื้นผิวเมมเบรน หาก IGFBP-1 มีอยู่ในตัวอย่างมันจะสร้างความซับซ้อนด้วยแอนติบอดีต่อต้าน IGFBP-1 หลักที่ผันกับอนุภาคสี คอมเพล็กซ์จะถูกผูกมัดโดยแอนติบอดีต่อต้าน IGFBP-1 ครั้งที่สองที่เคลือบบนเยื่อหุ้มไนโตรเซลลูโลส การปรากฏตัวของสายทดสอบที่มองเห็นได้พร้อมกับสายควบคุมจะบ่งบอกถึงผลลัพธ์ที่เป็นบวก
ส่วนประกอบชุด
| 20 p implบ้า pกกED อุปกรณ์ทดสอบ | อุปกรณ์แต่ละตัวมีแถบที่มีคอนจูเกตสีและรีเอเจนต์ปฏิกิริยาที่เคลือบล่วงหน้าในภูมิภาคที่สอดคล้องกัน |
| 2การสกัดขวดบัฟเฟอร์ | 0.1 M ฟอสเฟตบัฟเฟอร์น้ำเกลือ (PBS) และ 0.02% โซเดียมอะไซด์ |
| 1 swab ควบคุมเชิงบวก (ตามคำขอเท่านั้น) | มี IGFBP-1 และโซเดียมอะไซด์ สำหรับการควบคุมภายนอก |
| 1 swab ควบคุมเชิงลบ (ตามคำขอเท่านั้น) | ไม่มี IGFBP-1 สำหรับการควบคุมภายนอก |
| 20 ท่อสกัด | สำหรับการใช้งานตัวอย่าง |
| 1 เวิร์คสเตชั่น | สถานที่สำหรับถือขวดบัฟเฟอร์และหลอด |
| 1 แพ็คเกจแทรก | สำหรับคำแนะนำในการดำเนินการ |
วัสดุที่จำเป็น แต่ไม่ได้จัดเตรียมไว้
| ตัวจับเวลา | สำหรับการใช้เวลา |
ข้อควรระวัง
■สำหรับมืออาชีพในการวินิจฉัยในหลอดทดลองเท่านั้น
■อย่าใช้หลังจากวันหมดอายุที่ระบุไว้ในแพ็คเกจ อย่าใช้การทดสอบหากกระเป๋าฟอยล์เสียหาย อย่านำการทดสอบกลับมาใช้ซ้ำ
■ชุดนี้มีผลิตภัณฑ์ที่มาจากสัตว์ ความรู้ที่ได้รับการรับรองเกี่ยวกับแหล่งกำเนิดและ/หรือสถานะสุขาภิบาลของสัตว์ไม่ได้รับประกันว่าจะไม่มีตัวแทนที่ทำให้เกิดโรคที่ถ่ายทอดได้ทั้งหมด ดังนั้นจึงขอแนะนำให้ผลิตภัณฑ์เหล่านี้ได้รับการปฏิบัติที่อาจติดเชื้อและจัดการกับการสังเกตข้อควรระวังด้านความปลอดภัยตามปกติ (ไม่กินหรือหายใจเข้า)
■หลีกเลี่ยงการปนเปื้อนข้ามของชิ้นงานโดยใช้คอนเทนเนอร์เก็บตัวอย่างใหม่สำหรับแต่ละตัวอย่างที่ได้รับ
■อ่านขั้นตอนทั้งหมดอย่างรอบคอบก่อนทำการทดสอบใด ๆ
■อย่ากินดื่มหรือควันในพื้นที่ที่มีการจัดการตัวอย่างและชุดอุปกรณ์ จัดการตัวอย่างทั้งหมดราวกับว่ามีสารติดเชื้อ สังเกตข้อควรระวังที่จัดตั้งขึ้นเพื่อต่อต้านอันตรายทางจุลชีววิทยาตลอดกระบวนการและปฏิบัติตามขั้นตอนมาตรฐานสำหรับการกำจัดตัวอย่างที่เหมาะสม สวมชุดป้องกันเช่นเสื้อโค้ทในห้องปฏิบัติการถุงมือที่ใช้แล้วทิ้งและการป้องกันดวงตาเมื่อทำการทดสอบตัวอย่าง
■อย่าแลกเปลี่ยนหรือผสมรีเอเจนต์จากล็อตที่แตกต่างกัน อย่าผสมฝาครอบขวดสารละลาย
■ความชื้นและอุณหภูมิอาจส่งผลเสียต่อผลลัพธ์
■เมื่อขั้นตอนการทดสอบเสร็จสิ้นให้กำจัด swabs อย่างระมัดระวังหลังจากการนึ่งพวกเขาที่ 121 ° C เป็นเวลาอย่างน้อย 20 นาที อีกวิธีหนึ่งคือพวกเขาสามารถรักษาด้วยโซเดียมไฮโปคลอไรด์ 0.5% (หรือฟอกขาวที่บ้าน) เป็นเวลาหนึ่งชั่วโมงก่อนการกำจัด วัสดุทดสอบที่ใช้แล้วควรถูกยกเลิกตามกฎระเบียบท้องถิ่นรัฐและ/หรือรัฐบาลกลาง
■อย่าใช้แปรง cytology กับผู้ป่วยที่ตั้งครรภ์
การจัดเก็บและความมั่นคง
■ชุดควรเก็บไว้ที่ 2-30 ° C จนกว่าวันหมดอายุที่พิมพ์ลงบนกระเป๋าปิดผนึก
■การทดสอบจะต้องอยู่ในกระเป๋าที่ปิดสนิทจนกว่าจะใช้งาน
■อย่าแช่แข็ง
■ควรใช้ความระมัดระวังเพื่อปกป้องส่วนประกอบในชุดนี้จากการปนเปื้อน อย่าใช้หากมีหลักฐานการปนเปื้อนของจุลินทรีย์หรือการตกตะกอน การปนเปื้อนทางชีวภาพของอุปกรณ์จ่ายตู้คอนเทนเนอร์หรือรีเอเจนต์สามารถนำไปสู่ผลลัพธ์ที่ผิดพลาด
การเก็บรวบรวมและจัดเก็บตัวอย่าง
ใช้เฉพาะ Dacron หรือ Rayon Tipped Sterile Swabs กับเพลาพลาสติก ขอแนะนำให้ใช้ SWAB ที่จัดทำโดยผู้ผลิตชุดอุปกรณ์ (SWABS ไม่ได้อยู่ในชุดนี้สำหรับข้อมูลการสั่งซื้อโปรดติดต่อผู้ผลิตหรือผู้จัดจำหน่ายในพื้นที่หมายเลขแคตตาลจ์คือ 207000) swabs จากซัพพลายเออร์รายอื่นยังไม่ได้รับการตรวจสอบ ไม่แนะนำให้ใช้คำแนะนำสำหรับผ้าฝ้ายหรือเพลาไม้
■ตัวอย่างที่ได้รับโดยใช้ Swab โพลีเอสเตอร์ที่ผ่านการฆ่าเชื้อ ตัวอย่างควรรวบรวมก่อนทำการตรวจสอบดิจิตอลและ/หรืออัลตร้าซาวด์ transvaginal ระวังอย่าให้สัมผัสอะไรกับ Swab ก่อนที่จะรับตัวอย่าง ใส่ปลายสุดของไม้กวาดเข้าไปในช่องคลอดอย่างระมัดระวังไปทางด้านหลัง fornix จนกว่าจะมีความต้านทาน อีกทางเลือกหนึ่งสามารถนำตัวอย่างจากด้านหลัง fornix ระหว่างการตรวจ speculum ที่ผ่านการฆ่าเชื้อ Swab ควรทิ้งไว้ในช่องคลอดเป็นเวลา 10-15 วินาทีเพื่อให้สามารถดูดซับการหลั่งในช่องคลอด ดึง swab ออกอย่างระมัดระวัง!.
■ใส่ swab ไปที่หลอดสกัดหากการทดสอบอาจทำงานได้ทันที หากไม่สามารถทดสอบได้ทันทีตัวอย่างผู้ป่วยควรวางไว้ในหลอดขนส่งแห้งสำหรับการจัดเก็บหรือการขนส่ง swabs อาจถูกเก็บไว้ 24 ชั่วโมงที่อุณหภูมิห้อง (15-30 ° C) หรือ 1 สัปดาห์ที่ 4 ° C หรือไม่เกิน 6 เดือนที่ -20 ° C ตัวอย่างทั้งหมดควรได้รับอนุญาตให้ไปถึงอุณหภูมิห้อง 15-30 ° C ก่อนการทดสอบ
ขั้นตอน
นำการทดสอบตัวอย่างบัฟเฟอร์และ/หรือควบคุมอุณหภูมิห้อง (15-30 ° C) ก่อนการใช้งาน
■วางท่อสกัดที่สะอาดในพื้นที่ที่กำหนดของเวิร์กสเตชัน เพิ่มบัฟเฟอร์การสกัด 1 มล. ลงในหลอดสกัด
■ใส่ตัวอย่าง Swab ลงในหลอด ผสมผสานสารละลายอย่างแรงโดยการหมุน Swab อย่างแรงที่ด้านข้างของหลอดเป็นเวลาอย่างน้อยสิบครั้ง (ในขณะที่จมอยู่ใต้น้ำ) ผลลัพธ์ที่ดีที่สุดจะได้รับเมื่อชิ้นงานผสมอย่างแรงในการแก้ปัญหา
■บีบของเหลวให้มากที่สุดเท่าที่จะเป็นไปได้จาก SWAB โดยการบีบด้านข้างของท่อสกัดที่ยืดหยุ่นเมื่อ SWAB ถูกลบออก อย่างน้อย 1/2 ของสารละลายบัฟเฟอร์ตัวอย่างจะต้องอยู่ในหลอดเพื่อให้การย้ายถิ่นของเส้นเลือดฝอยเพียงพอที่จะเกิดขึ้น ใส่ฝาลงบนหลอดสกัด
ทิ้ง SWAB ในภาชนะขยะที่เหมาะสมทางชีวภาพที่เหมาะสม
■ตัวอย่างที่สกัดสามารถรักษาไว้ที่อุณหภูมิห้องเป็นเวลา 60 นาทีโดยไม่ส่งผลกระทบต่อผลการทดสอบ
■ถอดการทดสอบออกจากกระเป๋าที่ปิดสนิทและวางไว้บนพื้นผิวที่สะอาดและระดับ ติดฉลากอุปกรณ์ด้วยผู้ป่วยหรือการควบคุม เพื่อให้ได้ผลลัพธ์ที่ดีที่สุดควรทำการทดสอบภายในหนึ่งชั่วโมง
■เพิ่มตัวอย่างสกัด 3 หยด 3 หยด (ประมาณ 100 ไมโครลิตร) จากหลอดสกัดไปยังตัวอย่างที่ดีบนเทปเทส
หลีกเลี่ยงการดักจับฟองอากาศในชิ้นงานชิ้นงานและอย่าวางสารละลายใด ๆ ในหน้าต่างสังเกตการณ์
เมื่อการทดสอบเริ่มทำงานคุณจะเห็นการเคลื่อนที่สีข้ามเมมเบรน
■รอให้แถบสีปรากฏขึ้น ผลลัพธ์ควรอ่านในเวลา 5 นาที อย่าตีความผลลัพธ์หลังจาก 5 นาที
ทิ้งหลอดทดสอบที่ใช้แล้วและเทปทดสอบในภาชนะสูญเปล่าทางชีวภาพที่เหมาะสม
การตีความผลลัพธ์
| เชิงบวกผลลัพธ์:
| สองแถบสีปรากฏบนเมมเบรน วงหนึ่งปรากฏขึ้นในภูมิภาคควบคุม (C) และอีกวงปรากฏขึ้นในภูมิภาคทดสอบ (T) |
| เชิงลบผลลัพธ์:
| มีแถบสีเดียวเท่านั้นที่ปรากฏในพื้นที่ควบคุม (C) ไม่มีแถบสีที่ชัดเจนปรากฏขึ้นในภูมิภาคทดสอบ (T) |
| ไม่ถูกต้องผลลัพธ์:
| วงควบคุมไม่ปรากฏ ผลลัพธ์จากการทดสอบใด ๆ ที่ไม่ได้สร้างแถบควบคุมในเวลาการอ่านที่ระบุจะต้องถูกยกเลิก โปรดตรวจสอบขั้นตอนและทำซ้ำด้วยการทดสอบใหม่ หากปัญหายังคงอยู่ให้หยุดการใช้ชุดทันทีและติดต่อผู้จัดจำหน่ายในพื้นที่ของคุณ |
บันทึก:
1. ความเข้มของสีในภูมิภาคทดสอบ (t) อาจแตกต่างกันไปขึ้นอยู่กับความเข้มข้นของสารที่มีจุดมุ่งหมายในตัวอย่าง แต่ระดับสารไม่สามารถกำหนดได้โดยการทดสอบเชิงคุณภาพนี้
2. ปริมาณตัวอย่างไม่เพียงพอขั้นตอนการทำงานที่ไม่ถูกต้องหรือการทดสอบที่หมดอายุเป็นเหตุผลที่เป็นไปได้มากที่สุดสำหรับความล้มเหลวของวงควบคุม
การควบคุมคุณภาพ
■การควบคุมขั้นตอนภายในรวมอยู่ในการทดสอบ แถบสีที่ปรากฏในภูมิภาคควบคุม (C) ถือเป็นการควบคุมขั้นตอนเชิงบวกภายใน มันยืนยันปริมาณตัวอย่างที่เพียงพอและเทคนิคขั้นตอนที่ถูกต้อง
■การควบคุมขั้นตอนภายนอกอาจให้ (ตามคำขอเท่านั้น) ในชุดอุปกรณ์เพื่อให้แน่ใจว่าการทดสอบนั้นทำงานได้อย่างถูกต้อง นอกจากนี้การควบคุมอาจใช้เพื่อแสดงประสิทธิภาพที่เหมาะสมโดยผู้ประกอบการทดสอบ ในการดำเนินการทดสอบการควบคุมเชิงบวกหรือเชิงลบให้ทำตามขั้นตอนในส่วนขั้นตอนการทดสอบที่รักษา SWAB ควบคุมในลักษณะเดียวกับ Swab ตัวอย่าง
ข้อ จำกัด ของการทดสอบ
1. ไม่ควรตีความเชิงปริมาณตามผลการทดสอบ
2. อย่าใช้การทดสอบหากกระเป๋าอลูมิเนียมฟอยล์หรือซีลของกระเป๋าไม่เหมือนเดิม
3.a Strongstep เชิงบวก®ผลการทดสอบพรหมแม้ว่าการตรวจจับการปรากฏตัวของน้ำคร่ำในตัวอย่างไม่ได้ค้นหาที่ตั้งของการแตก
4. ด้วยการทดสอบการวินิจฉัยทั้งหมดผลลัพธ์จะต้องตีความในแง่ของผลการวิจัยทางคลินิกอื่น ๆ
5. หากการแตกของเยื่อหุ้มทารกในครรภ์เกิดขึ้น แต่การรั่วไหลของของเหลวน้ำคร่ำได้หยุดลงมากกว่า 12 ชั่วโมงก่อนที่ตัวอย่างจะถูกนำมาใช้ IGFBP-1 อาจถูกย่อยสลายโดยโปรตีเอสในช่องคลอดและการทดสอบอาจให้ผลลัพธ์เชิงลบ
ลักษณะประสิทธิภาพ
ตาราง: Strongstep®การทดสอบพรหมกับการทดสอบพรหมอีกแบรนด์อื่น
|
ความไวสัมพัทธ์: |
| แบรนด์อื่น |
| ||
| + | - | ทั้งหมด | |||
| StrongStep®พรอม ทดสอบ | + | 63 | 3 | 66 | |
| - | 2 | 138 | 140 | ||
|
| 65 | 141 | 206 | ||
ความไวในการวิเคราะห์
ปริมาณที่ตรวจพบได้ต่ำสุดของ IGFBP-1 ในตัวอย่างที่สกัดคือ 12.5 μg/L
สารรบกวน
ต้องใช้ความระมัดระวังเพื่อไม่ให้ปนเปื้อนสารคัดหลั่งของแอปพลิเคชันหรือ cervicovaginal ด้วยน้ำมันหล่อลื่นสบู่น้ำยาฆ่าเชื้อหรือครีม น้ำมันหล่อลื่นหรือครีมอาจรบกวนการดูดซึมของชิ้นงานลงบนแอปพลิเคชัน สบู่หรือฆ่าเชื้ออาจรบกวนปฏิกิริยาแอนติบอดี-แอนติเจน
สารรบกวนที่มีศักยภาพได้รับการทดสอบที่ความเข้มข้นที่อาจพบได้อย่างสมเหตุสมผลในการหลั่ง cervicovaginal สารต่อไปนี้ไม่ได้รบกวนการทดสอบเมื่อทดสอบในระดับที่ระบุ
| สาร | ความเข้มข้น | สาร | ความเข้มข้น |
| ampicillin | 1.47 มก./มล. | Prostaglandin F2 | 0.033 mg/ml |
| erythromycin | 0.272 mg/ml | Prostaglandin E2 | 0.033 mg/ml |
| ไตรมาสที่ 3 ปัสสาวะของมารดา | 5% (ฉบับ) | Monistatr (miconazole) | 0.5 มก./มล. |
| ออกซิโตซิน | 10 IU/ml | สีคราม | 0.232 mg/ml |
| Terbutaline | 3.59 มก./มล. | คนอื่น ๆ | 0.849 mg/ml |
| dexamethasone | 2.50 มก./มล. | เจล Betadiner | 10 มก./มล. |
| MGSO4-7H2O | 1.49 มก./มล. | Betadiner Cleanser | 10 มก./มล. |
| ริน | 0.33 mg/ml | K-yy Jelly | 62.5 มก./มล. |
| Dermicidolr 2000 | 25.73 mg/ml |
การอ้างอิงวรรณกรรม
Erdemoglu และ Mungan T. ความสำคัญของการตรวจจับปัจจัยการเจริญเติบโตคล้ายอินซูลินที่มีผลผูกพันโปรตีน -1 ในการหลั่ง cervicovaginal: เปรียบเทียบกับการทดสอบ nitrazine และการประเมินปริมาณน้ำคร่ำ Acta Obstet Gynecol Scand (2004) 83: 622-626
Kubota T และ Takeuchi H. การประเมินผลของปัจจัยการเจริญเติบโตที่คล้ายอินซูลินจับโปรตีน -1 เป็นเครื่องมือวินิจฉัยสำหรับการแตกของเยื่อหุ้มเซลล์ J Obstet Gynecol Res (1998) 24: 411-417
Rutanen Em et al. การประเมินผลการทดสอบแถบอย่างรวดเร็วสำหรับปัจจัยการเจริญเติบโตที่มีลักษณะคล้ายอินซูลินจับโปรตีน -1 ในการวินิจฉัยของเยื่อหุ้มทารกในครรภ์ที่แตก Clin Chim Acta (1996) 253: 91-101
Rutanen EM, Pekonen F, Karkkainen T. การวัดปัจจัยการเจริญเติบโตคล้ายอินซูลินที่มีผลผูกพันโปรตีน -1 ในการหลั่งปากมดลูก/ช่องคลอด: เปรียบเทียบกับอิมมูโนเมมเบรนตรวจสอบ ROM ในการวินิจฉัยเยื่อหุ้มเซลล์ของทารกในครรภ์ที่แตก Clin Chim Acta (1993) 214: 73-81
อภิธานศัพท์ของสัญลักษณ์
|
| หมายเลขแคตตาล็อก |  | ข้อ จำกัด อุณหภูมิ |
 | ปรึกษาคำแนะนำสำหรับการใช้งาน |
| รหัสแบทช์ |
 | ในอุปกรณ์การแพทย์วินิจฉัยในหลอดทดลอง |  | ใช้โดย |
 | ผู้ผลิต |  | มีเพียงพอสำหรับ |
 | อย่านำกลับมาใช้ใหม่ |  | ตัวแทนที่ได้รับอนุญาตในประชาคมยุโรป |
 | CE ทำเครื่องหมายตาม IVD Medical Devices Directive 98/79/EC | ||